 На рак почки в структуре онкологических заболеваний приходится около 4%. По темпам прироста онкологической заболеваемости в России почечно-клеточный рак (ПКР) устойчиво занимает у женщин третье место после рака полости рта и глотки и центральной нервной системы (ЦНС), а у мужчин – четвертое место после рака предстательной и щитовидной желез и ЦНС. Ежегодно в России от рака почки умирают более 8 тыс. человек. Стандартизованный показатель заболеваемости населения России злокачественными опухолями почки составляет 8,09 на 100 тыс. населения [1]. Рост заболеваемости раком почки частично обусловлен как улучшением диагностики на основе современных инструментальных исследований, таких как трансабдоминальное ультразвуковое исследование (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), так и ростом истинной заболеваемости раком почки. В настоящее время в 25–40% случаев заболевание выявляют случайно при профилактическом обследовании. Мужчины болеют в 2 раза чаще, чем женщины, в основном на 5–7-м десятилетии жизни. Частота почечно-клеточного рака постепенно увеличивается. Пятилетняя выживаемость при этой патологии достигает 60%. Однако при наличии метастазов 2-летняя выживаемость колеблется от 0 до 20%. От 25 до 50% больных имеют метастазы на момент установления диагноза. Более того, приблизительно у половины больных после радикальной нефрэктомии впоследствии появляются метастазы.
На рак почки в структуре онкологических заболеваний приходится около 4%. По темпам прироста онкологической заболеваемости в России почечно-клеточный рак (ПКР) устойчиво занимает у женщин третье место после рака полости рта и глотки и центральной нервной системы (ЦНС), а у мужчин – четвертое место после рака предстательной и щитовидной желез и ЦНС. Ежегодно в России от рака почки умирают более 8 тыс. человек. Стандартизованный показатель заболеваемости населения России злокачественными опухолями почки составляет 8,09 на 100 тыс. населения [1]. Рост заболеваемости раком почки частично обусловлен как улучшением диагностики на основе современных инструментальных исследований, таких как трансабдоминальное ультразвуковое исследование (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), так и ростом истинной заболеваемости раком почки. В настоящее время в 25–40% случаев заболевание выявляют случайно при профилактическом обследовании. Мужчины болеют в 2 раза чаще, чем женщины, в основном на 5–7-м десятилетии жизни. Частота почечно-клеточного рака постепенно увеличивается. Пятилетняя выживаемость при этой патологии достигает 60%. Однако при наличии метастазов 2-летняя выживаемость колеблется от 0 до 20%. От 25 до 50% больных имеют метастазы на момент установления диагноза. Более того, приблизительно у половины больных после радикальной нефрэктомии впоследствии появляются метастазы.
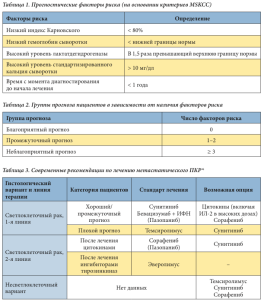
Ангиогенез является одним из ключевых патогенетических механизмов роста злокачественного новообразования и диссеминации опухолевого процесса, в связи с чем одними из основных целей противоопухолевой таргетной терапии являются внутриклеточные мишени, вовлеченные в процесс стимуляции ангиогенеза и опухолевого роста. В настоящее время разработано несколько препаратов, влияющих на разные внутриклеточные мишени, относящиеся к патогенетическому пути, связанному с инактивацией гена VHL. Сунитиниб – таблетированный ингибитор тирозинкиназ, который воздействует на все известные виды рецепторов к PDGF и VEGF (VEGFRs, PDGFR-a, PDGFR-b, c-KIT и FLT-3), участвующих в процессе роста опухоли, патологическом ангиогенезе и метастазировании. Препарат был одобрен в Европе с 2007 г. в качестве первой и второй линий терапии распространенного рака почки и в настоящее время рекомендован в качестве стандарта лечения больных с благоприятным и промежуточным прогнозом заболевания по критериям MSKCC (Memorial Sloan-Kettering Cancer Center) (табл. 1). Основываясь на числе имеющихся факторов риска, R.J. Motzer и соавт. [2, 3] предложили стратифицировать больных на три группы прогноза (табл. 2). На основании проведенных многоцентровых международных исследований [4–6] была разработана и предложена тактика проведения лечения данной болезни в зависимости от группы прогноза (табл. 3).
Материалы и методы
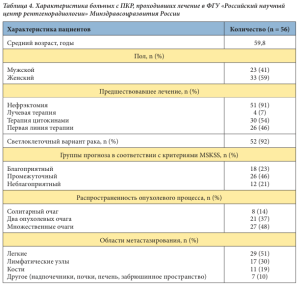
В ФГУ «Российский научный центр рентгенорадиологии» Минздравсоцразвития России было проведено лечение 56 больных с распространенным почечно-клеточным раком, которые получали сунитиниб в качестве лекарственной терапии. Характеристика пациентов приведена в таблице 4. У 13 (23%) больных распространенный процесс выявлен до хирургического этапа лечения, в связи с чем операция носила циторедуктивный характер. Четыре (7%) пациента получали дистанционную лучевую терапию по поводу болевого синдрома. Прогрессирование заболевания в сроки от 1 года до 5 лет зарегистрировано у 31 (55%) больного.
Терапия проводилась в стандартном режиме: сунитиниб – 50 мг в сутки 1 раз в день в режиме «4/2» (4 недели лечения с последующим перерывом в течение 2 недель). В связи с развитием нежелательных явлений доза сунитиниба была снижена до 37,5 мг/ сут у 11 (20%) пациентов. Лечение было временно приостановлено у 2 (4%) пациентов из-за развития нежелательных явлений 3-й степени тяжести и затем возобновлено после их купирования. Терапия проводилась до подтвержденного прогрессирования заболевания, развития выраженных побочных эффектов или прекращения приема по желанию пациента.
Мониторинг выполнялся каждые 30 дней. При визитах выявлялись нежелательные явления, проводились лабораторные исследования: биохимический анализ крови (глюкоза, билирубин общий, щелочная фосфатаза, аланиновая трансаминаза, аспарагиновая трансаминаза, мочевина, креатинин, коагулограмма), общий анализ мочи. Один раз в 3 месяца выполнялась КТ грудной клетки, брюшной полости, органов малого таза с болюсным усилением; один раз в 6 месяцев – остеосцинтиграфия, по показаниям – электрокардиограмма, при наличии клинических проявлений – КТ головного мозга.
Результаты
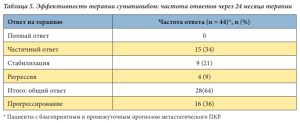
Представлен анализ результатов лечения сунитинибом для пациентов с благоприятным и промежуточным прогнозом заболевания в первой и второй линии терапии (n = 44). Через 24 месяца терапии частичный ответ зарегистрирован у 15 (34%) из 44 больных, стабилизация – у 9 (20%) и регрессия – у 4 (9%). Помимо этого, у 12 (27%) больных отмечена стабилизация в течение 15 месяцев, у 4 (9%) больных – стабилизация в течение 9 месяцев с последующим прогрессированием заболевания (табл. 5). Шесть больных погибли в течение первых шести месяцев лечения. Данные больные относились к группе неблагоприятного прогноза метастатичес- кого ПКР, имели множественные метастазы, в большинстве случаев – костные.
Основными побочными действиями препарата были повышение артериального давления, диарея, слабость. Степень тяжести побочных действий не превышала 2-й. Все побочные действия хорошо контролировались и медикаментозно купировались.
Обсуждение результатов
В процессе применения сунитиниба в стандартном режиме первой и второй линии терапии ПКР нами было выявлено, что безрецидивная выживаемость в общей исследуемой популяции больных почечно-клеточным раком в среднем составила 13 месяцев, общая выживаемость – 22 месяца. Было показано, что результаты терапии сунитинибом лучше в группе пациентов с единичными паренхиматозными метастазами, чем у больных, имеющих метастазы в кости и/или множественные метастатические очаги (> 2).
Выводы
Применение сунитиниба у больных ПКР увеличивает общую и безрецидивную выживаемость. Терапия сунитинибом редко осложняется развитием выраженных нежелательных явлений (3–4-й степени тяжести), требующих проведения специального лечения и/или отмены проводимой терапии, и в целом хорошо переносится.
Авторы: к.м.н. А.А. Клименко, д.м.н., проф. А.Д. Каприн, д.м.н. А.Ю. Павлов, к.м.н. С.А. Иванов. ФГУ «Российский научный центр рентгенорадиологии» Минздравсоцразвития России, РУДН, кафедра урологии с курсом онкоурологии, Городская клиническая больница No 20
Литература:
1. Чиссов В.И., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2007 г. М., 2008.
2. Motzer R.J., Bacik J., Murphy B.A. et al. Interferon-alfa as a comparative treatment for clinical trials of new therapies against advanced renal cell carcinoma // J. Clin. Oncol. 2002. Vol. 20. No 1. P. 289–296.
3. Motzer R.J., Hutson T.E., Tomczak P. et al. Sunitinib versus interferon alfa in metastatic renal-cell carcinoma // N. Engl. J. Med. 2007. Vol. 356. No 2. P. 115–124.
4. Feldman D.R., Kondagunta G.V., Ronnen E.A. et al. Phase I trial of be- vacizumab plus sunitinib in patients (pts) with metastatic renal cell carcinoma (mRCC) // J. Clin. Oncol. 2009. Vol. 27. No 9. P. 1432–1439.
5. Минимальные клинические рекомендации Европейского общества медицинской онкологии (ESMO) / под ред. С.А. Тюляндина, Д.А. Носова, Н.И. Переводчикова. М.: Издательская группа РОНЦ им. Н.Н. Блохина РАМН, 2010. 436 с.
6. Giberti C., Oneto F., Martorana G. et al. Radical nephrectomy for renal cell carcinoma: long-term results and prognostic factors on a series of 328 cases // Eur. Urol. 1997. Vol. 31. No 1. P. 40–48