 Успешная чрескожная нефролитотрипсия (ЧНЛТ) зависит от адекватного дооперационного планирования и оптимального осуществления чрескожного доступа. КТ в настоящее время стала стандартной визуализирующей методикой при выполнении ЧНЛТ. В отношении чрескожного доступа к почке, КТ может быть использована для планирования доступа, произведения доступа и для наблюдения за пациентом после осуществления доступа. В этом обзоре мы обсуждаем значение каждого аспекта для чрескожного доступа в почке при ЧНЛТ. В частности, мы описываем технику получения доступа при помощи КТ, ценную методику при сложном строении чашечно-лоханочной системы.
Успешная чрескожная нефролитотрипсия (ЧНЛТ) зависит от адекватного дооперационного планирования и оптимального осуществления чрескожного доступа. КТ в настоящее время стала стандартной визуализирующей методикой при выполнении ЧНЛТ. В отношении чрескожного доступа к почке, КТ может быть использована для планирования доступа, произведения доступа и для наблюдения за пациентом после осуществления доступа. В этом обзоре мы обсуждаем значение каждого аспекта для чрескожного доступа в почке при ЧНЛТ. В частности, мы описываем технику получения доступа при помощи КТ, ценную методику при сложном строении чашечно-лоханочной системы.
Введение
Успешная чрескожная нефролитотрипсия (ЧНЛТ) основывается на адекватном дооперационном планировании и оптимальном осуществлении чрескожного доступа. В этом отношении, качество информации лучевых методов, предоставляемой хирургу, является ключевым. Массив конкремента и его соотношение с чашечно-лоханочной системой должны быть отображены для выбора оптимального чрескожного доступа к почке и внутрипочечного хода, которые обеспечивали бы возможность максимального удаления конкремента с минимальной травмой для паренхимы [1]. Также должны быть установлены точные пространственные соотношения с другими хирургическими ориентирами, такими как ребра и органы брюшной полости.
Мультиспиральная компьютерная томография (МСКТ) произвела революцию в радиологической диагностике заболевания мочевой системы. [2] Специализированная нативная и контрастная КТ является более точной по сравнению с ультразвуковым исследованием и контрастной рентгенографией методикой для диагностики мочекаменной болезни. [3] Применительно к перкутанному доступу при хирургическом лечении нефролитиаза, КТ имеет еще большие преимущества, такие как определение анатомических аномалий внутренних органов или оценку пространственного соотношения плевры и места доступа. В случае чрескожного доступа, КТ может быть использована для его планирования, проведения, и в периоде после осуществления доступа. В этом обзоре, мы обсуждаем роль каждого аспекта для ЧНЛТ. В частности, мы описываем технику получения доступа при помощи КТ, ценную методику при сложном строении чашечно-лоханочной системы.
КТ для планирования чрескожного доступа к почке. Нативная КТ
Преимущества дооперационной нативной КТ (нКТ) включают определение положения периферических конкрементов в передних и задних чашечках, направления чашечных отрогов коралловидных камней, оценку толщины паренхимы над конкрементами и визуализацию конкрементов с низкой рентгеновской плотностью, плохо видимых на обзорных снимках [4]. Контрастная одноплоскостная радиография традиционно была стандартом для планирования ЧНЛТ, потому что конфигурация собирательной системы не может быть установлена при аксиальной КТ. В сравнение, главное преимущество аксиальной КТ заключается в ее способности определять анатомические аномалии. Аксиальную КТ следует рутинно использовать у пациентов с удвоением почки из-за высокой частоты позадипочечного расположения ободочной кишки. [5]. Так же, возможность визуализации сосудистых структур и кишечника сделала ее стандартной методикой при планировании доступа к трансплантированной [6] или эктопически расположенной почке [7].
Совсем недавно, был описан новый метод прогнозирования успешности рентгеноскопического доступа к верхнему полюсу через подреберный либо надреберный доступ при помощи аксиальной КТ. [8]. Измеренные при КТ расстояния от кожи до камня и от камня до первого среза, не содержащего ребра, были использованы для вычисления угла поворота рентгеновской дуги от надреберного к подреберному положению. В этом исследовании величина угла более 30 градусов прогнозировала неудачу рентгеноскопического надреберного доступа с положительной и отрицательной прогностической точностью 100% и 76,4% соответственно.
Разработка спиральной КТ с элиминацией дыхательных артефактов облегчило реконструкцию изображения с сопутствующим анализом соседних анатомических структур для осуществления доступа. Исследования сагиттальных реконструкций в положении на спине и на животе показали более высокую безопасность надреберного доступа при положении пациента на животе. Риск повреждения плевры в различных фазы дыхания также был оценен в этом исследовании; риск повреждения плевры при доступе над 12 ребром по сравнению с доступом над 11 ребром был меньше на 66-82%, если доступ производился на полном выдохе. В противоположность, на риск повреждения плевры при доступе к верхнему полюсу почки над 11-ребром фаза дыхания влияния не оказывала, и он был недопустимо высок (83%). [9]
Также оценивала нативная трехмерная реконструкция коралловидных камней для планирования доступа. [10-12]. В определенных случаях 3D-КТ-реконструкция конкрементов почки может помочь в определении места доступа и интраоперационной ориентации. 10. В одном исследовании, у трети пациентов место доступа изменялось по сравнению с таковым, если бы была использованы соответствующие аксиальные КТ-сканы и экскреторная урография. 11. Тем не менее, не все исследования сходятся на преимуществах данного метода в планировании доступа. 12. Это может быть отражением ограниченности топографических данных при реконструкции конкрементов без окружающей чашечно-лоханочной системы.
В более новых исследованиях нКТ для планирования чрескожного доступа использовались технологии трехмерной реконстрункции, такие как многоплоскостное реформирование (МПР). Эта методика способна производить оценку волюметрических данных в любой плоскости и использовалась для определения экстра/трансперионеального доступа к верхнему полюсу в обеих фазах дыхании при положении пациента на животе. 13. При использовании этого метода, могут быть созданы предпосылки для альтернативных доступов, таких как лапароскопия. Дальнейшее исследование, в котором использовалось МПР для планирования доступа к нижней чашечке, показало, что аксиальные КТ-сканы переоценивают риск повреждения ободочной кишки в сравнении с косыми парасагиттальными реформациями. 14. Мы рутинно получаем нативные мультипланарные реформации в положении на животе для определения риска повреждения внутренних органов и плевры при планировании чрескожного доступа.
КТ-пиелография.
Трехмерная КТ-реконструкция контрастированной чашечно-лоханочной системы способна обеспечить четкое представление переднезадней ориентации чашечек, информации, трудной для определения при экскреторной урографии. 15. Тем не менее, первые исследования имели ограниченную ценность для планирования доступа, потому что конкременты были неотличимы от контрастного препарата. 15. С этим ограничением сейчас пытаются справиться, используя МСКТ и совершенствуя методику КТ.
В исследовании 10 пациентов с камнями почек, трехмерные реконструкции контрастированной ЧЛС помогли определить двух пациентов, у которых выполнение ЧНЛТ было невозможным вследствие неудачного расположения камня по отношению к ЧЛС. 16. Среди пациентов, которым проводилась ЧНЛТ, трехмерная КТ-урография (3D-КТУ) оказалось полезной в выборе места чрескожного доступа. Также, 3D-КТУ использовалась для планирования сложных доступов, например при подковообразной почке. 17. В этом случае, для планирования доступа использовался видеофрагмент объемной реконструкции, вращающейся на 360 градусов. Видеофрагменты делают более легким определение пространственных соотношений ЧЛС и камня и обеспечиваются ясную оценку углов входа, а также их соотношение с ребрами. Эти реконструкции могут быть загружены на подключенные к сети компьютеры для просмотра в операционной во время хирургического вмешательства.
Недавно оценивалась точность протокола целенаправленной трехмерной КТ-пиелографии для визуализации конкрементов почек при планировании чрескожного доступа. 18. В этом исследовании у 20 пациентов, которым планировалось выполнение ЧНЛТ, 3D-КТУ в положении на животе позволяла точно определить положение камня и его соотношение с чашечно-лоханочной системой. Реконструкции проекций максимальной интенсивности были оптимальными для отображения конкрементов, в то время как объемные реконструкции были лучшими в отношении анатомии чашечно-лоханочной системы. Трехмерная КТ-пиелография обладает способностью визуализации параллельных чашечек с камнями, изображения ориентации чашечек и сжатости суженных чашечек или шейки дивертикулов чашечки. 18. В таблице 1 приведены важные фактов, которые необходимо иметь в виду при планировании доступа с использованием КТ. Примеры планирования доступа с использованием трехмерной КТ пиелографии показаны на рисунках 1 и 2.
КТ для проведения чрескожного доступа к почке.
Двух плоскостная рентгеноскопия и ультрасонография, самостоятельно либо в сочетании с рентгеноскопия, являются наиболее часто используемыми методами визуализации при проведении доступа для ЧНЛТ. 19,20. Однако, в определенных случаях, КТ-контролируемый доступ может быть единственным выбором, потому что он предоставляет точную кросс-секционную визуализацию, при помощи которой может быть достигнута пункция собирательной системы.
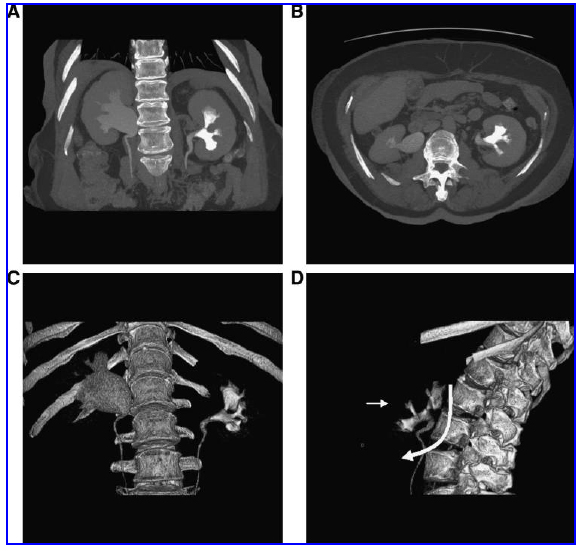
Риск 1. Коронарная и аксиальная проекции максимальной интенсивности (A,B) и объемные реконструкции (C, D) коралловидного камня левой почки. Хотя на аксиальном и коронарном сканах виден камень, планирование доступа к почке будет более точным при объемной реконструкции. Латеральный вид взят из видеофрагмента и показывает, что почка «провалена» в заднем направлении. Доступ к верхнему полюсу обеспечил бы легкую навигацию от верхнего к нижнему полюсу (изогнутая стрелка) через почечную лоханку, но латеральная (межполюсная) чашечка (прямая стрелка) отходит под острым углом. С точки зрения планирования, это может означать необходимость второй прямой пункции для удаления камня, но так как она является независимой чашечкой, у пациента возможно использований вспомогательной ударно-волновой литотрипсии для резидуальных фрагментов в этой чашечке.
Показания для КТ-контролируемого доступа.
Техника КТ-контролируемого чрескожного доступа к почке были впервые описана Haaga с соавт 21 в 1977 г. Показания для КТ-контролируемого доступа включают анатомические аномалии, такие как спинальная дизрафия 22, морбидное ожирение, аномалии внутренних органов (позадипочечное расположение кишечника или селезенки) 22, аномальную анатомии мочевого тракта (отведения мочи) 23, аномальную анатомию почки (множественные кисты, ангиомиолипома) 24, эктопическую/трасплантированную почку и неудачный доступ при использовании обычной рентгеноскопии/ультрасонографии. Последнее может происходить при отсутствии дилатации ЧЛС, когда визуализация собирательной системы не выполнима с использованием ретроградного (например, стриктура мочеточника) или внутривенного (обструкция/почечная недостаточность) контрастирования.
Техника.
КТ-контролируемый чрескожный доступ к почке может быть осуществлен в интервенционной радиологической операционной, оснащенной томографом, с использованием КТ «в реальном времени» 25 или в сочетании с КТ-рентгеноскопией 26. В качестве альтернативы, возможно выполнение доступа в обычном КТ-кабинете с промежуточными сканами при выходе хирурга из кабинета. 27. Последний метод позволяет избежать лучевой нагрузки на врача. Некоторые исследователи также использовали лазерные системы наведения для облегчения входа иглы 25. Доступ осуществляется в положении пациента на животе, либо в положении косо/на спине. Последний может иметь преимущества у пациентов с дыхательными нарушениями.
Изначально снимается ориентировочная томограмма для локализации области почек. Получается нативное изображение брюшной полости, оценивается наличие дилатации ЧЛС, присутствия опухолей почек, положения почек по отношению к ободочной кишке, селезенке, печени и диафрагме. Собирательная система должна быть хорошо различима при наличии ее дилатации. В случае отсутствия дилатации может потребоваться внутривенное введение контрастного вещества.
Производится идентификация подходящей для пункции чашечки, при этом следуют принципу, что игла пересекается свод задней чашечки, потому что это снижает риск артериального кровотечения по сравнению со вход через воронку или лоханку. 28. Метки на коже могут быть размещены над выбранным место пункции, последующее сканирование может помочь в репозиции меток таким образом, чтобы они располагались над целевой чашечкой в поперечной плоскости. 21. Локализация сканов в области интереса уменьшает лучевую нагрузку.
Когда поперечной положение иглы подтверждено, кожа стерилизуется и обкладывается стерильными простынями. 15-сантиметровая 18-калиберная игла с кожухом (например, игла Келлета, Rocket Medical, Watford, Herts, UK), используется для обеспечения местно анестезии и проводится подкожно. Следующее локализующее сканирование с кончиком иглы, фиксированным на месте, может помочь в определении ее положения по отношению к целевой чашечке. На основании этого сканирования, траектория иглы и изменяется и она проводится либо вперед либо назад до получения мочи. Полезной может быть аспирация при манипуляциях иглы.
Иногда для получения доступа к ЧЛС требуется от двух до трех сканировании. Часто необходимо только провести иглу вперед или назад на несколько миллиметров, чтобы попасть в нужную чашечку. Когда по иглы начинает выделяться моча, повторное сканирование подтверждает положение иглы в собирательной системе. Затем стилет иглы удаляется, и струна через кожух проводится в собирательную систему. Кожух удаляется, и небольшой надрез кожи позволяет последовательно проводиться расширение хода. Расширение хода может происходит при помощи только КТ, либо стандартным способом с использованием рентгеноскопии и антеградным введением контрастного вещества.
В чашечно-лоханочную систему устанавливается нефростомическая трубка, и последующее сканирование подтверждает ее положение, а также исключает местные осложнения. Трубка подшивается к коже и пациент переводится для последующей ЧНЛТ. На рис.3 показан пример, когда КТ-наведение было использовано для доступа к ЧЛС.
Исходы
В большинстве исследований по КТ-контролируемому доступу оценивалось размещение нефростомической трубки при различных показаниях, включая ЧНЛТ (25-27,29). Результаты крупных исследований просуммированы в таблице 2. Неудача чрескожного доступа при КТ-контроле является редкостью, и в некоторых исследованиях сообщается о 100% успешного доступа (27,29). Частота незначимых осложнений варьирует от 1% до 14%, о серьезных осложнениях не упоминается. Дилатированные ЧЛС ассоциируются с меньшим риском осложнений, временем выполнения процедуры и необходимостью повторных пункций. 29. В серии шести КТ-контролируемых пункций для ЧНЛТ, произведенных Matlaga с соавт., 22 не было неудачных доступов и осложнений. Общий показатель полного клиренса конкрементов составил 83%.
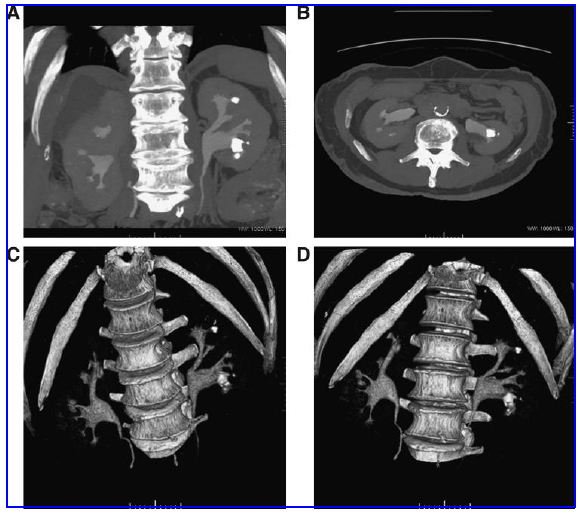
Рис 2. Коронарная и аксиальная проекции максимальной интенсивности (ПМИ) (А, В) и объемные реконструкции (С, Д) компьютерной томографий смешанных оксалатных камней в нескольких чашечках левой почки. На ПМИ хорошо видны все конкременты, но пространственные соотношения с ЧЛС могут польностью оценены только на объемных реконструкциях, а именно в видеофрагменте вращающейся реконструкции. Камни нижнего полюса находятся в смещенной относительно вперед чашечке, шейка ее широкая, в то время как шейка верхней чашечки узкая и угол между лоханкой и этой шейкой относительно острый. Более того, верхний конкремент находится в узкой латерально ориентированной чашечке. Принимая это во внимание, был произведен доступ к нижней чашечке, камни удалены при помощи ригидного нефроскопа 24 Ch, камень верхней чашечки удален при помощи гибкого нефроскопа №12 Ch и корзинки. Полный клиренс конкрементов был достигнут через один доступ.
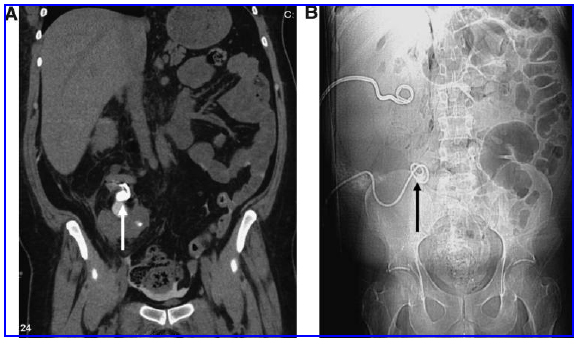
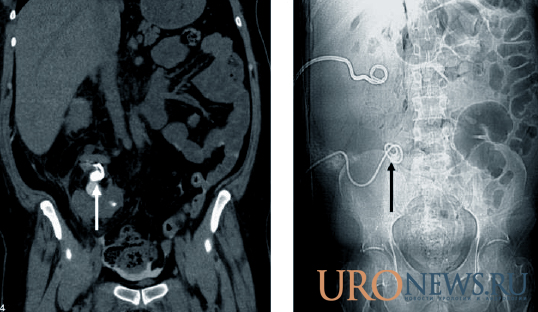
Рис. 3. Мультипланарная реформация КТ (А) и обзорный снимок брюшной полости (В) у пациента с удвоением перекрестно-эктопированной почки и камня в обеих почках. На коронарном изображении видна нефростомическая трубка, установленная для досутпа к нижнему полюсу под контролем КТ с целью избежания перфорации брюшины. Камень, указанный стрелкой, прилежит к проксимальному концу нефростомического дренажа. На соответствующем обзорном снимке камень также указан стрелкой (камень ортотопической почки уже удален).
КТ после чрескожного доступа
Сканирование сразу же после произведения КТ-контролируемого доступа может исключить значимые осложнения. Более того, при КТ можно обнаружить и устранить неправильное расположение нефростомической трубки. Рентгеноскопия при наличии перфорации лоханки может привести к «заливанию» проекции ЧЛС контрастом, что усложняет манипуляции с нефростомимическим дренажем. При использовании КТ, нефростомический дренаж может быть репозиционирован в ЧЛС путем потягивания его на себя на расстояние его экструзии за пределы лоханки. 30.
Преимущество КТ в оценке локализации (интраренальной/экстраренальной) и размера резидуальных конкрементов (РК) после хирургии нефролитиаза является общепризнанным (4,31). Нативная МСКТ является золотым стандартом для определения РК после ЧНЛТ 32. В проспективном анализе антеградной пиелографии, рентгенографии почек, мочеточников и мочевого пузыря (РПММП) и нативной КТ после ЧНЛТ было обнаружено трехкратное снижение числа больных с полным клиренсом камней при использовании КТ для оценки наличия РК через 1 месяц. Резидуальные фрагменты, обнаруженные при КТ и невидимые при антеградной пиелографии и рентгенографии, обнаружены у 42% больных, их средний размер составил 7,6 мм. 33. Однако в более новом исследовании, сравнивавшем МСКТ с рентгенографией и линейной томографией, не было обнаружено статистически значимого увеличения чувствительности для плотных РК размером более 5 мм. 34. Это привело к формированию концепции «видимых при КТ клинических незначимых резидуальных конкрементов размером менее 5 мм». 34.
Вывод
Возможность и удобство реконструкции при МСКТ увеличило значимость КТ для чрескожного доступа к почке. Неконтрастные реформации могут обуславливать возможность связанных с доступов повреждение внутренних органов, требующих альтернативного места доступа или применения другой леченой опции. Трехмерная КТ-пиелография способна изобразить точное положение камней в ЧЛС и таким образом помочь в определении наиболее подходящей точки доступа для максимального клиренса конкрементов. Аксиальная КТ может быть использована для получения доступа в сложных случаях. После ЧНЛТ, КТ служит точным методом для определения местных осложнений, а также репозиции нефростомической трубки. Наконец, состояние резидуальных конкрементов после ЧНЛТ наилучшим образом оценивается при нативной КТ.
Источник: Khurshid R. Ghani, B.Sc. JOURNAL OF ENDOUROLOGY Volume 23, Number 10, October 2009 Mary Ann Liebert, Inc. Pp. 1633–1639. Department of 1Urology and Clinical Radiology, St George’s Hospital and Medical School, London, United Kingdom. Перевод: к.м.н. старший научный сотрудник НИИ Уронефрологии и репродуктивного здоровья человека И.П. Матюхов, аспирант кафедры урологии ПМГМУ им. Сеченова Восканян Г.Э.
Литература:
1. Park S, Pearle MS. Imaging for percutaneous renal access and management of renal calculi. Urol Clin North Am 2006; 33:353–364.
2. Chow LC, Sommer FG. Multidetector CT urography with abdominal compression and three-dimensional reconstruction. AJR Am J Roentgenol 2001;177:849–855.
3. Smith RC, Rosenfield AT, Choe KA, Essenmacher KR, Verga M, Glickman MG, Lange RC. Acute flank pain: Comparison of non-contrast–enhanced CT and intravenous urography. Radiology 1995;194:789–794.
4. Wickham JE, Fry IK, Wallace DM. Computerised tomography localisation of intrarenal calculi prior to nephrolithotomy. Br J Urol 1980;52:422–425.
5. Skoog SJ, Reed MD, Gaudier FA Jr, Dunn NP. The posterolateral and the retrorenal colon: Implication in percutaneous stone extraction. J Urol 1985;134:110–112.
6. Krambeck AE, Leroy AJ, Patterson DE, Gettman MT. Percutaneous nephrolithotomy success in the transplant kidney. J Urol 2008;180:2545–2549.
7. Watterson JD, Cook A, Sahajpal R, Bennett J, Denstedt JD. Percutaneous nephrolithotomy of a pelvic kidney: A posterior approach through the greater sciatic foramen. J Urol 2001;166:209–210.
8. Bilen CY, Koc¸ak B, Kitirci G, Danaci M, Sarikaya S. Simple trigonometry on computed tomography helps in planning renal access. Urology 2007;70:242–245.
9. Hopper KD, Yakes WF. The posterior intercostal approach for percutaneous renal procedures: Risk of puncturing the lung, spleen, and liver as determined by CT. AJR Am J Roentgenol 1990;154:115–117.
10. Buchholz NP. Three-dimensional CT scan stone reconstruction for the planning of percutaneous surgery in a morbidly obese patient. Urol Int 2000;65:46–48.
11. Hubert J, Blum A, Cormier L, Claudon M, Regent D, Mangin P. Three-dimensional CT-scan reconstruction of renal calculi. A new tool for mapping-out staghorn calculi and follow-up of radiolucent stones. Eur Urol 1997;31:297– 301.
12. Liberman SN, Halpern EJ, Sullivan K, Bagley DH. Spiral computed tomography for staghorn calculi. Urology 1997; 50:519–524.
13. Ng CS, Herts BR, Streem SB. Percutaneous access to upper pole renal stones: Role of prone 3-dimensional computerized tomography in inspiratory and expiratory phases. J Urol 2005;173:124–126.
14. Tuttle DN, Yeh BM, Meng MV, Breiman RS, Stoller ML, Coakley FV. Risk of injury to adjacent organs with lowerpole fluoroscopically guided percutaneous nephrostomy: Evaluation with prone, supine, and multiplanar reformatted CT. J Vasc Interv Radiol 2005;16:1489–1492.
15. Heyns CF, van Gelderen WF. 3-dimensional imaging of the pelviocaliceal system by computerized tomographic reconstruction. J Urol 1990;144:1335–1338.
16. Thiruchelvam N, Mostafid H, Ubhayakar G. Planning percutaneous nephrolithotomy using multidetector computed tomography urography, multiplanar reconstruction and three-dimensional reformatting. BJU Int 2005;95:1280–1284.
17. Ghani KR, Rintoul M, Patel U, Anson K. Three-dimensional planning of percutaneous renal stone surgery in a horseshoe kidney using 16-slice CT and volume-rendered movies. J Endourol 2005;19:461–463.
18. Patel U, Walkden RM, Ghani KR, Anson K. Threedimensional CT pyelography for planning of percutaneous
nephrostolithotomy: Accuracy of stone measurement, stone depiction and pelvicalyceal reconstruction. Eur Radiol
2009;19:1280–1288.
19. Miller NL, Matlaga BR, Lingeman JE. Techniques for fluoroscopic percutaneous renal access. J Urol 2007;178:15–23.
20. Osman M, Wendt-Nordahl G, Heger K, Michel MS, Alken P, Knoll T. Percutaneous nephrolithotomy with
ultrasonography-guided renal access: Experience from over 300 cases. BJU Int 2005;96:875–878.
21. Haaga JR, Zelch MG, Alfidi RJ, Stewart BH, Daugherty JD. CT-guided antegrade pyelography and percutaneous nephrostomy. AJR Am J Roentgenol 1977;128:621–624.
22. Matlaga BR, Shah OD, Zagoria RJ, Dyer RB, Streem SB, Assimos DG. Computerized tomography guided access for percutaneous nephrostolithotomy. J Urol 2003;170:45–47.
23. Davis WB, Trerotola SO, Johnson MS, et al. Percutaneous imaging-guided access for the treatment of calculi in continent urinary reservoirs. Cardiovasc Intervent Radiol 2002;
25:119–122.
24. Eiley DM, Ozsvath B, Siegel DN, Smith AD. Percutaneous nephrolithotomy with renal angiomyolipomas: A rare challenge.
J Endourol 1999;13:27–30.
25. LeMaitre L, Mestdagh P, Marecaux-Delomez J, Valtille P, Dubrulle F, Biserte J. Percutaneous nephrostomy: Placement under laser guidance and real-time CT fluoroscopy. Eur Radiol 2000;10:892–895.
26. Barbaric ZL, Hall T, Cochran ST, Heitz DR, Schwartz RA, Krasny RM, Deseran MW. Percutaneous nephrostomy: Placement under CT and fluoroscopy guidance. AJR Am J Roentgenol 1997;169:151–155.
27. Thanos L, Mylona S, Stroumpouli E, Kalioras V, Pomoni M, Batakis N. Percutaneous CT-guided nephrostomy: A safe and quick alternative method in management of obstructive and nonobstructive uropathy. J Endourol 2006;20:486–490.
28. Sampaio FJ, Zanier JF, Araga˜o AH, Favorito LA. Intrarenal access: 3-dimensional anatomical study. J Urol 1992;148: 1769–1773.
29. Egilmez H, Oztoprak I, Atalar M, et al. The place of computed tomography as a guidance modality in percutaneous nephrostomy: Analysis of a 10-year single-center experience.
Acta Radiol 2007;48:806–813.
30. Jones CD, McGahan JP. Computed tomographic evaluation and guided correction of malpositioned nephrostomy catheters.
Abdom Imaging 1999;24:422–425.
31. Pearle MS, Watamull LM, Mullican MA. Sensitivity of noncontrast helical computerized tomography and plain film radiography compared to flexible nephroscopy for detecting residual fragments after percutaneous nephrostolithotomy. J Urol 1999;162:23–26.
32. Halachmi S, Ghersin E, Ginesin Y, Meretyk S. Antegrade pyelography versus unenhanced multidetector CT in the assessment of urinary-tract stones after percutaneous nephrostomy insertion: A prospective blinded study. J Endourol2007;21:473–477.
33. Park J, Hong B, Park T, Park HK. Effectiveness of noncontrast computed tomography in evaluation of residual